*仅供医学专业人士阅读参考天创网

糖尿病治疗新突破与胰岛β细胞再生的未来前景。
整理:医学界报道组
审核:洪天配教授
糖尿病已成为全球公共卫生的重大挑战。据世界卫生组织统计,全球糖尿病患者数量已突破4亿,且仍在不断攀升。糖尿病的危害不仅局限于升高,还可引发多种长期并发症,严重影响患者的生活质量。在这样的背景下,GLP-1受体激动剂逐渐成为备受瞩目的治疗选择。这类药物在有效降低血糖的同时,还被证实对心血管、肾脏、肝脏等器官/系统具有保护作用,并能帮助患者减轻体重等益处,始终吸引着医生和患者的广泛关注。
2025年8月,北京大学第三医院内分泌科主任洪天配教授在中华医学会第二十二次内分泌学学术会议(CSE)上,就“GLP-1受体激动剂对胰岛β细胞的影响:改善功能还是延缓衰竭?”这一前沿议题作了主旨报告。作为长期致力于糖尿病基础与临床研究的知名专家,洪教授不仅系统回顾了该类药物的临床应用历程,更结合最新研究进展,着重探讨了其在改善胰岛β细胞功能、促进β细胞再生潜力方面的机制与未来前景。
GLP-1改善2型糖尿病患者胰岛β细胞功能:从临床证据到机制阐释
洪天配教授首先系统回顾了胰高糖素样肽-1(GLP-1)受体激动剂在2型糖尿病治疗中改善胰岛β细胞功能的多项临床研究[1-3]。他指出,这类药物不仅可实现良好的血糖控制,更具备保护甚至修复β细胞功能的潜力。洪教授强调,“GLP-1受体激动剂通过葡萄糖浓度依赖的方式促进胰岛素分泌,抑制胰高糖素释放,减轻β细胞凋亡,并改善胰岛素生物合成与胰岛素原剪切为成熟胰岛素,综合发挥其胰岛保护效应[4]。”
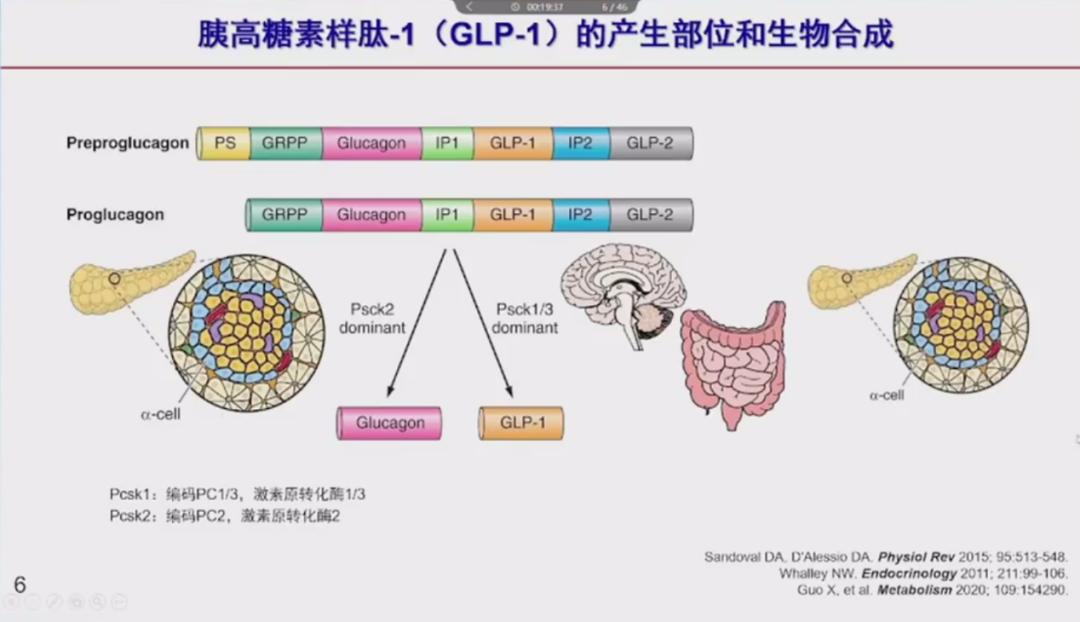
图1 胰高糖素原的生物合成与GLP-1的组织特异性加工路径示意图
一项为期6个月的多中心临床研究显示[5],接受GLP-1受体激动剂治疗的患者HOMA-β指数显著升高、胰岛素原/胰岛素比值显著降低,提示β细胞功能明显改善。尤其在与传统口服降糖药对比中,GLP-1药物在血糖控制的稳定性及β细胞应答方面表现更优,且这一效益在长期治疗中仍得以维持。
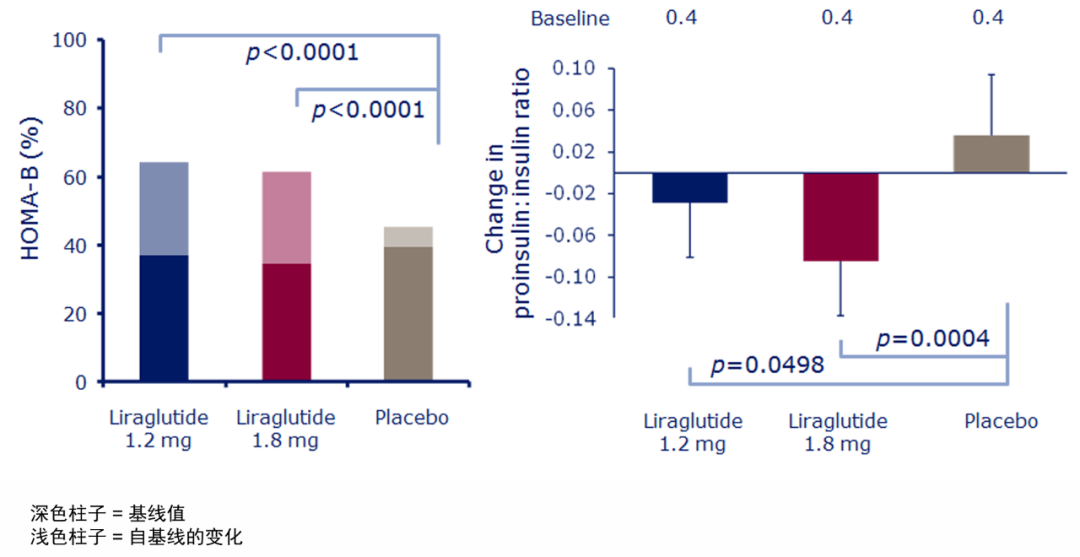
图2 利拉鲁肽改善β细胞功能:HOMA-b指数升高与胰岛素原/胰岛素比值降低
在机制方面,洪教授详细介绍了其团队的研究发现[6-7]:GLP-1受体激动剂可通过激活cAMP-PKA信号通路,上调激素原转化酶PC1/3和PC2的表达和活性,从而提高成熟胰岛素生成效率,增强β细胞应对血糖波动的能力。
GLP-1在动物模型中促进β细胞再生的证据与机制探索
洪教授进一步从动物实验角度,阐述了GLP-1受体激动剂在胰岛β细胞再生方面的作用。他指出,早在2020年[8],已有研究显示艾塞那肽干预可显著增加2型糖尿病模型GK大鼠的β细胞总量。近年来更多实验表明天创网 ,GLP-1不仅抑制β细胞凋亡,还可促进β细胞增殖、诱导胰岛α细胞向β细胞。
值得注意的是,洪教授团队开展了一系列探索胰高糖素信号阻断对β细胞再生影响的研究。通过使用胰高糖素受体(GCGR)的阻断性单克隆抗体[9-10],他们发现抑制胰高糖素信号不仅引起α细胞代偿性增生,还促使α细胞分泌更多的胰高糖素和GLP-1,两者通过激活GLP-1受体(GLP-1R)及其下游信号发挥旁分泌调节效应,从而促进β细胞的再生与功能恢复。这一发现揭示了一条新型的α-β细胞轴调控通路,为理解GLP-1/GLP-1R系统在胰岛自我修复中的作用提供了新视角。
洪教授还指出[9-10],在2型糖尿病模型小鼠中,使用GCGR阻断剂可显著增加胰高糖素/胰岛素双阳性细胞数量,提示存在胰岛α细胞向β细胞转分化的可能性。通过谱系示踪实验,其团队证实这一转分化现象确实存在。此外,他们进一步发现β细胞再生还涉及胰腺内分泌前体细胞来源的β细胞新生、β细胞自我复制等路径。
GLP-1对人类β细胞再生潜力的研究进展与临床转化前景
尽管临床前结果令人振奋,GLP-1是否真正促进人类胰岛β细胞再生仍是学界关切的焦点。洪教授详细介绍了一项2020年发表于《
Science Translational Medicine》的重要研究,其中指出 GLP-1受体激动剂与DYRK1A抑制剂联合使用,可显著提升人类 原代 胰岛的 β细胞增殖能力。
该研究团队进一步在免疫缺陷小鼠模型中开展人类胰岛移植的实验,结果显示,艾塞那肽联合哈玛尼碱(DYRK1A抑制剂)[11]治疗不仅改善糖耐量,还显著增加胰岛移植物β细胞的数量和增殖能力。尤其重要的是,早期干预(移植后即开始治疗)显示出优于延迟治疗(胰岛移植物再血管化后开始治疗)的促进β细胞再生效应,提示治疗时机对改善β细胞疗效具有决定性影响。
洪教授强调,“这些发现虽然仍处于临床前阶段,但为β细胞再生治疗提供了坚实的科学依据与联合用药的新策略。”他同时提醒,要实现真正的临床转化,仍需更多设计严谨、长期随访的随机对照试验加以验证。
超越血糖控制:GLP-1的多重效益与未来发展方向
洪教授在总结中强调,GLP-1受体激动剂的价值远不止于血糖控制。他指出,该类药物的作用涉及中枢食欲抑制、能量代谢调节、体脂分布调控乃至心肾保护等多个方面,是具有多维度效益的“代谢调节剂”。
此外,洪教授还展望了未来研究方向,包括探索GLP-1与其他靶点药物[如SGLT2抑制剂、葡萄糖依赖性促胰岛素多肽(GIP)受体激动剂]的协同效应,开发口服或更长效制剂,以及利用生物标志物筛选优势应答人群等。他认为,“唯有真正理解其系统生物学效应,才能最大化GLP-1受体激动剂的临床获益潜力。”
小结
洪天配教授的报告全面而深入地总结了GLP-1和GLP-1受体激动剂在胰岛β细胞保护作用与β细胞再生领域的最新进展,从临床疗效到底层机制,从动物实验到人类胰岛研究初步证据,为与会者提供了一场学术盛宴。
最后,洪教授表示,GLP-1受体激动剂的研究仍在快速发展之中,其未来不仅作为降糖药物,更有望成为疾病修正疗法(Disease-modifying therapy)的核心组成部分天创网 ,最终改变2型糖尿病的自然病程。
专家简介

洪天配教授
北京大学第三医院内分泌科主任、教授、主任医师、博导
北京大学内分泌代谢学系主任
中国医师协会内分泌代谢科医师分会候任会长、中华医学会内分泌学分会副主任委员(第9-11届)等
牵头制订中华人民共和国卫生行业标准《糖尿病筛查和诊断》。中文核心期刊发表论文400余篇。
JAMADiabetesDiabetologiaMetabolismCell Metab等期刊发表SCI论文100余篇
参考文献:
[1] Sandoval DA, D'Alessio DA. Physiology of proglucagon peptides: role of glucagon and GLP-1 in health and disease. Physiol Rev. 2015 Apr;95(2):513-48. doi: 10.1152/physrev.00013.2014. PMID: 25834231.
[2] Whalley NM, Pritchard LE, Smith DM, White A. Processing of proglucagon to GLP-1 in pancreatic α-cells: is this a paracrine mechanism enabling GLP-1 to act on β-cells? J Endocrinol. 2011 Oct;211(1):99-106. doi: 10.1530/JOE-11-0094. Epub 2011 Jul 27. PMID: 21795304.
[3] Pridal L, Deacon CF, Kirk O, Christensen JV, Carr RD, Holst JJ. Glucagon-like peptide-1(7-37) has a larger volume of distribution than glucagon-like peptide-1(7-36)amide in dogs and is degraded more quickly in vitro by dog plasma. Eur J Drug Metab Pharmacokinet. 1996 Jan-Mar;21(1):51-9. doi: 10.1007/BF03190278. PMID: 8839678.
[4] Wei T, Cui X, Jiang Y, Wang K, Wang D, Li F, Lin X, Gu L, Yang K, Yang J, Hong T, Wei R. Glucagon Acting at the GLP-1 Receptor Contributes to β-Cell Regeneration Induced by Glucagon Receptor Antagonism in Diabetic Mice. Diabetes. 2023 May 1;72(5):599-610. doi: 10.2337/db22-0784. PMID: 36826938; PMCID: PMC10130488.
[5] Zinman B, Gerich J, Buse JB, Lewin A, Schwartz S, Raskin P, Hale PM, Zdravkovic M, Blonde L; LEAD-4 Study Investigators. Efficacy and safety of the human glucagon-like peptide-1 analog liraglutide in combination with metformin and thiazolidinedione in patients with type 2 diabetes (LEAD-4 Met+TZD). Diabetes Care. 2009 Jul;32(7):1224-30. doi: 10.2337/dc08-2124. Epub 2009 Mar 16. Erratum in: Diabetes Care. 2010 Mar;33(3):692. PMID: 19289857; PMCID: PMC2699702.
[6] Ding J, Gao Y, Zhao J, Yan H, Guo SY, Zhang QX, Li LS, Gao X. Pax6 haploinsufficiency causes abnormal metabolic homeostasis by down-regulating glucagon-like peptide 1 in mice. Endocrinology. 2009 May;150(5):2136-44. doi: 10.1210/en.2008-1006. Epub 2008 Dec 30. PMID: 19116343.
[7] Wen JH, Chen YY, Song SJ, Ding J, Gao Y, Hu QK, Feng RP, Liu YZ, Ren GC, Zhang CY, Hong TP, Gao X, Li LS. Paired box 6 (PAX6) regulates glucose metabolism via proinsulin processing mediated by prohormone convertase 1/3 (PC1/3). Diabetologia. 2009 Mar;52(3):504-13. doi: 10.1007/s00125-008-1210-x. Epub 2008 Nov 26. PMID: 19034419.
[8] Holst JJ, Gasbjerg LS, Rosenkilde MM. The Role of Incretins on Insulin Function and Glucose Homeostasis. Endocrinology. 2021 Jul 1;162(7):bqab065. doi: 10.1210/endocr/bqab065. PMID: 33782700; PMCID: PMC8168943.
[9] Wei R, Gu L, Yang J, Yang K, Liu J, Le Y, Lang S, Wang H, Thai D, Yan H, Hong T. Antagonistic Glucagon Receptor Antibody Promotes α-Cell Proliferation and Increases β-Cell Mass in Diabetic Mice. iScience. 2019 Jun 28;16:326-339. doi: 10.1016/j.isci.2019.05.030. Epub 2019 May 30. PMID: 31203188; PMCID: PMC6581654.
[10] Lang S, Wei R, Wei T, Gu L, Feng J, Yan H, Yang J, Hong T. Glucagon receptor antagonism promotes the production of gut proglucagon-derived peptides in diabetic mice. Peptides. 2020 Sep;131:170349. doi: 10.1016/j.peptides.2020.170349. Epub 2020 Jun 16. PMID: 32561493.
[11] Ackeifi C, Wang P, Karakose E, Manning Fox JE, González BJ, Liu H, Wilson J, Swartz E, Berrouet C, Li Y, Kumar K, MacDonald PE, Sanchez R, Thorens B, DeVita R, Homann D, Egli D, Scott DK, Garcia-Ocaña A, Stewart AF. GLP-1 receptor agonists synergize with DYRK1A inhibitors to potentiate functional human β cell regeneration. Sci Transl Med. 2020 Feb 12;12(530):eaaw9996. doi: 10.1126/scitranslmed.aaw9996. PMID: 32051230; PMCID: PMC9945936.
责任编辑丨小林
*\"医学界\"力求所发表内容专业、可靠,但不对内容的准确性做出承诺;请相关各方在采用或以此作为决策依据时另行核查。

辉煌配资提示:文章来自网络,不代表本站观点。